Россия
Россия
acidophilus в рационах трех экономически значимых видов рыб в Ираке: тепловодных – обыкновенного карпа (Cyprinus carpio) и нильской тиляпии (Oreochromis niloticus) – и холодноводной радужной форели (Oncorhynchus mykiss). В ходе 90-дневного эксперимента рыба содержалась в садках и получала либо контрольный рацион, либо рацион, обогащенный пробиотиком на основе Lactobacillus acidophilus. Оценивались показатели роста, эффективность использования корма, химический состав тела и микробиологический профиль кишечника. Результаты продемонстрировали статистически высокодостоверное (P < 0,001) улучшение всех производственных показателей в группах с применением пробиотического корма. Удельная скорость роста (SGR) увеличилась на 18,9–21,3 %, а коэффициент конверсии корма (FCR) снизился на 15,9–18,8 % в зависимости от вида. Наблюдалось значительное увеличение содержания белка (на 9,5–10,3 %) и жира (на 15,4–17,2 %) в организме рыб. По результатам микробиологического анализа установлено, что произошло резкое увеличение популяции молочнокислых бактерий и подавление условно-патогенной микрофлоры (более 98 %) в просвете кишечника рыб, получавших пробиотик, что положительно отразилось на физиологическом состоянии организма рыбы. Таким образом, препарат на основе Lactobacillus acidophilus является высокоэффективной кормовой добавкой, способствующей улучшению роста, повышению эффективности кормления и модуляции кишечной микробиоты, и может быть рекомендован для устойчивого развития рыбоводства в Ираке. В контексте аквакультуры Ирака, сталкивающейся с вызовами в виде высокой стоимости кормов и необходимости повышения устойчивости производства, применение данного пробиотика представляет собой практически значимую и экологически безопасную стратегию.
пробиотики, аквакультура, карп, тиляпия, радужная форель, Ирак, показатели роста, кормовая эффективность, качество воды
Введение
Сектор аквакультуры в Ираке сталкивается со значительными экологическими и экономическими проблемами, такими как нехватка воды, высокая стоимость кормов и распространение болезней. В ответ на эти вызовы срочно необходимы инновационные решения для повышения эффективности производства. Одним из таких многообещающих инструментов стали пробиотики. В 2001 г. Продовольственная и сельскохозяйственная организация (ФАО) и Всемирная организация здравоохранения (ВОЗ) определили их как «живые микроорганизмы, которые при введении в достаточных количествах приносят пользу здоровью хозяина» [1]. В Ираке широко культивируются карп (Cyprinus carpio), тиляпия (Oreochromis spp.) и радужная форель (Oncorhynchus mykiss). По данным Министерства сельского хозяйства Ирака, на долю карпа приходится более 70 % производства рыбы в стране [2]. Пробиотики, в состав которых входят полезные штаммы бактерий Lactobacillus и Bacillus, благотворно действуют на здоровье рыб с помощью нескольких механизмов. Они способствуют пищеварению и снижают распространенность заболеваний [3, 4]. Кроме того, бактерии действуют, выделяя пищеварительные ферменты (амилазу и протеазу), которые повышают степень усвоения питательных веществ. Они также стимулируют выработку антител и иммунных клеток, таких как макрофаги, укрепляя иммунитет рыб [5]. Пробиотики также улучшают качество воды за счет уменьшения накопления аммиака и нитритов, создавая более благоприятную среду для роста рыбы [6]. Они также конкурируют с патогенными микробами, колонизируя стенки кишечника и ограничивая активность вредных бактерий [3]. Тиляпия хорошо подходит для южных водоемов Ирака. Исследование в провинции Ди-Кар показало, что применение пробиотиков на водной основе с Pseudomonas fluorescens снизило распространенность грибковых заболеваний на 60 % [7]. Разведение радужной форели сосредоточено в горных районах северного Ирака. Исследования в Курдистане продемонстрировали, что добавление L. rhamnosus в корм для форели улучшило усвоение белка на 18 % и снизило стресс у рыб во время транспортировки и обработки [5, 8]. Данное исследование направлено на изучение применения пробиотиков в технологии разведения ключевых для Ирака видов рыб: карпа, тиляпии и форели. Цель работы – оценить эффективность пробиотиков в повышении продуктивности, снижении заболеваемости. Из всестороннего обзора исследований последних лет следует, что специалисты приходят к устойчивому пониманию эффективности применения пробиотиков в аквакультуре. Особое внимание в этих работах уделено показателям роста, укреплению иммунитета и устойчивости к болезням [9]. Например, Ahmadifar et al. показали, что Lactobacillus fermentum и феруловая кислота синергетически усиливают иммунные реакции у обыкновенного карпа [2]. Последующая работа Ahmadifar et al. расширила это понимание, в работе изучено регуляторное воздействие растительных экстрактов и пробиотических составов на иммунную систему и репродуктивную функцию рыб [10–12]. Понимание действия пробиотиков значительно продвинулось благодаря работе Ajdari et al., которые систематически сравнивали различные пищевые добавки (PrimaLac, инулин и Biomin Imbo) у обыкновенного карпа, демонстрируя их дифференцированное воздействие на антиоксидантные и иммунные реакции [7]. Аналогичным образом Akanmu et al. предоставили важные сведения о защитных эффектах Lactobacillus fermentum и Saccharomyces cerevisiae против Aeromonas hydrophila у Heterobranchus bidorsalis [13]. Assan et al. проанализировали данные о влиянии пробиотиков на пищеварительные ферменты у различных водных видов [9]. Были также проанализированы данные о влиянии пробиотиков на пищеварительные ферменты у рыб и моллюсков [14]. Совокупность данных этих исследований позволяет рекомендовать включение пробиотических стратегий в качестве устойчивых решений в современную практику аквакультуры [15–17].
Несмотря на эти положительные результаты, применению пробиотиков в Ираке препятствует ряд проблем, включая недостаточную техническую осведомленность фермеров, слабую инфраструктуру для местного производства и высокую стоимость импорта активных штаммов. Для решения этих проблем эксперты рекомендуют создавать специализированные исследовательские центры при иракских университетах, предоставлять фермерам субсидируемые государством пробиотики и развивать сотрудничество с международными организациями, такими как ФАО, для реализации пилотных проектов [1]. По мнению экспертов в области сельского хозяйства, данная биотехнология обладает потенциалом увеличить объем производства рыбы в Ираке до 500 000 т к 2030 г. Достижение этой цели потребует расширения сотрудничества между государственными структурами и частным сектором, а также увеличения инвестиций в прикладные исследования для эффективного переноса технологий из лабораторий на рыбные фермы [14].
Материалы и методы
Исследование проводилось в трех различных регионах Ирака, выбранных с учетом их специфических экологических и климатических условий, оптимальных для каждого вида рыб (табл. 1); эксперимент длился 125 суток: с 10 ноября 2024 г. по 15 марта 2025 г.
Таблица 1
Table 1
Места и условия выращивания исследуемых видов рыб
Places and conditions of cultivation of the studied fish species
|
Параметр |
Обыкновенный карп |
Нильская тиляпия |
Радужная форель |
|
Регион |
Округ Эль-Хилла, |
Провинция Басра |
Провинция Дахук, |
|
Источник воды |
Р. Евфрат (пресная вода) |
Р. Шатт-эль-Араб |
Оз. Дахук (холодная, |
|
Условия |
Плавучие садки |
Плавучие садки, установленные в водных каналах, отходящих от Шатт-эль-Араб |
Плавучие садки, установленные в озере |
|
Размеры садков, м |
1 × 1 × 2 |
1 × 1 × 2 |
1 × 1 × 2 |
В основе данного исследования лежал строго контролируемый экспериментальный дизайн, в котором было задействовано 18 садков (по 6 на каждый вид), разделенных на две основные группы: контрольную группу (3 садка в трехкратной повторности), получавшую стандартный корм, и опытную группу (3 садка в трехкратной повторности), получавшую корм, обогащенный пробиотиком. В каждый садок было помещено по 100 рыб со средним начальным весом 100 ± 2 г. Было приготовлено 2 вида изоэнергетических и изопротеиновых кормов. Использовались ингредиенты и рецептура в соответствии с указаниями фирмы-производителя – AgrFeed Iraq. Первый – контрольный корм, второй – пробиотический, содержащий лиофилизированную культуру Lactobacillus acidophilus в концентрации 1 × 109 КОЕ/г. Часть связующего вещества (целлюлозы) в контрольном корме была заменена на пробиотик в опытном корме. Состав кормов приведен в табл. 2.
Таблица 2
Table 2
Состав экспериментальных кормов, г/кг
Composition of experimental feeds, g/kg
|
Ингредиент |
Контрольный рацион |
Пробиотический рацион |
|
Рыбная мука |
400 |
|
|
Пшеничная мука |
363 |
|
|
Рыбий жир |
30 |
|
|
Витамины |
20 |
|
|
Минералы |
||
|
Пробиотик (L. acidophilus) |
0 |
10 |
|
Связующее вещество (целлюлоза) |
167 |
157 |
|
Итого |
1 000 |
|
Для приготовления корма сухие ингредиенты тщательно смешивали до получения гомогенной массы. Затем постепенно добавляли рыбий жир и воду до образования плотного теста. Тесто гранулировали с помощью экструдера. Полученные гранулы высушивали при комнатной температуре в течение 30 ч и хранили в прохладном, сухом месте до использования.
Кормление рыбы проводилось дважды в день (утром и вечером). Каждые две недели из садков отбиралась случайная выборка из 30 рыб для индивидуального взвешивания с целью мониторинга темпов роста. Взвешивание проводилось быстро, чтобы минимизировать стресс для рыбы. Оценка ростовых показателей проводилась с использованием стандартных ln [18, 19]:
Прирост массы, г = Средняя конечная масса – Средняя начальная масса;
Удельная скорость роста, сут.–1 =
= [(ln (Конечная масса) – ln (Начальная масса)) / Количество дней];
Кормовой коэффициент = Количество потребленного корма / Общий прирост массы;
Выживаемость, % = (Конечное количество рыб / Начальное количество рыб)  100.
100.
Основные параметры качества воды (температура, растворенный кислород, соленость и pH) измерялись еженедельно. Температура воды во время исследований варьировала в пределах 25–28 °C, содержание кислорода поддерживалось в пределах 6,5 мг/л, показатель рН – 7,8. Для поддержания температуры воды в оптимальном для радужной форели диапазоне (12–16 °C) в условиях жаркого климата Ирака использовались промышленные системы охлаждения (чиллеры) (рис. 1) и затеняющие сетки над садками для уменьшения воздействия прямых солнечных лучей (рис. 2).

Рис. 1. Промышленный чиллер для охлаждения воды в аквакультуре
Fig. 1. Industrial chiller for cooling water in aquaculture

Рис. 2. Затеняющие сетки над садками для снижения температуры воды
Fig. 2. Shading nets over cages to reduce water temperature
Проведен всесторонний статистический анализ для оценки влияния пробиотической добавки L. acidophilus на продуктивность и физиологические параметры трех ключевых видов аквакультуры. Статистическая обработка данных проводилась с использованием программного обеспечения SPSS (версия 25,0). Для оценки достоверности различий между средними значениями в контрольных и опытных группах для каждого вида рыб применялся t-критерий для независимых выборок. Различия считались статистически значимыми при уровне значимости P < 0,01.
Результаты исследования
Анализ показателей роста рыб и эффективности использования кормов. Первоочередной задачей анализа была оценка влияния пробиотика на основные показатели роста. В табл. 3 представлены сводные данные по приросту массы, относительной и удельной скоростям роста, коэффициенту конверсии корма и выживаемости.
Таблица 3
Table 3
Показатели роста рыб, получавших пробиотические и контрольные корма
Growth performance indicators of fish fed with probiotic and control diets
|
Вид рыбы |
Вариант |
Прирост массы, г |
Относительная скорость |
Удельная скорость роста, сут–1 |
Коэффициент конверсии корма FCR |
Выживаемость, % |
|
Обыкновенный карп |
Контроль |
150 |
50 |
1,5 |
1,8 |
85 |
|
Пробиотик |
180 |
60 |
1,8 |
1,5 |
90 |
|
|
Нильская |
Контроль |
120 |
45 |
1,3 |
1,9 |
80 |
|
Пробиотик |
150 |
55 |
1,6 |
1,6 |
88 |
|
|
Радужная |
Контроль |
200 |
60 |
1,7 |
1,6 |
90 |
|
Пробиотик |
230 |
70 |
2,0 |
1,3 |
95 |
Как следует из данных, представленных в табл. 3, рыбы, получавшие пробиотик, продемонстрировали превосходство по всем ключевым показателям. У радужной форели, например, удельная скорость роста увеличилась с 1,7 до 2,0 % в день, что является существенным ускорением производственного цикла. Наиболее важным с экономической точки зрения является значительное снижение коэффициента конверсии корма FCR у всех видов, особенно у форели (с 1,6 до 1,3). Это снижение на 18,8 % напрямую транслируется в сокращение затрат на корма, которые являются основной статьей расходов в аквакультуре. Кроме того, наблюдалось увеличение выживаемости на 5–8 %, что свидетельствует о благотворном влиянии пробиотика на общее состояние здоровья и стрессоустойчивость рыб. Для визуализации этих различий был построен график, представленный на рис. 3.
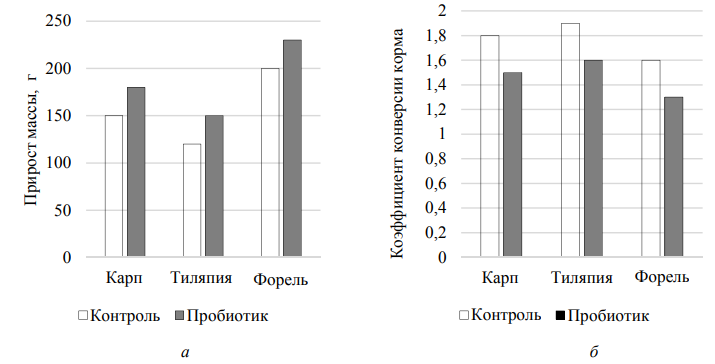
Рис. 3. Сравнение ключевых показателей продуктивности (прирост массы и FCR) у трех видов рыб
при контрольной и пробиотической обработке: а – прирост массы; б – коэффициент конверсии корма
Fig. 3. Comparison of key productivity indicators (weight gain and FCR) in three fish species during control
and probiotic treatment: a – weight gain; б – feed conversion rate
Согласно данным рис. 3 пробиотическая диета последовательно и значительно улучшает как рост, так и эффективность использования корма у всех исследованных видов.
Анализ химического состава тела рыб. Химический состав тела рыбы является интегральным показателем, отражающим не только качество корма, но и эффективность метаболических процессов. В табл. 4 представлены данные по содержанию основных компонентов в теле рыб в начале и в конце эксперимента.
Таблица 4
Table 4
Химический состав тела рыб, %, в начале и в конце эксперимента (на сырую массу)
Proximate chemical composition of fish body, %, at the start and end of the experiment (wet basis)
|
Вид рыбы |
Компонент |
Начало эксперимента |
Конец эксперимента |
|
|
контроль |
пробиотик |
|||
|
Обыкновенный карп |
Белок |
18,0 |
20,0 |
22,0 |
|
Жир |
5,0 |
6,0 |
7,0 |
|
|
Нильская тиляпия |
Белок |
17,5 |
19,5 |
21,5 |
|
Жир |
4,8 |
5,8 |
6,8 |
|
|
Радужная форель |
Белок |
19,0 |
21,0 |
23,0 |
|
Жир |
5,5 |
6,5 |
7,5 |
|
Данные табл. 4 свидетельствуют о том, что использование пробиотика привело к увеличению содержания белка и жира в тканях рыб. Например, содержание белка у карпа в опытной группе достигло 22,0 % по сравнению с 20,0 % в контроле. Это указывает на улучшенное переваривание и усвоение аминокислот из корма. Повышенное содержание жира свидетельствует об улучшении энергетического обмена и может положительно отразиться на вкусовых качествах и товарной ценности конечной продукции. Эти изменения напрямую связаны с улучшенной микрофлорой кишечника, способствующей более полному расщеплению питательных веществ, что наглядно показано на рис. 4.
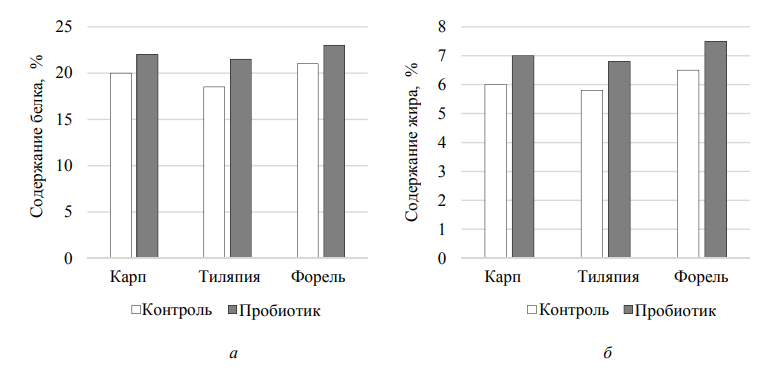
Рис. 4. Сравнение конечного содержания белка и жира у рыб контрольной и опытной групп:
а – содержание белка; б – содержание жира
Fig. 4. Comparison of the final protein and fat content in fish of the control and experimental groups:
a – protein content; б – fat content
Во всех случаях опытная группа демонстрировала более высокие уровни накопления белка и жира, подтверждая улучшение питательного статуса рыб (см. рис. 4).
Комплексный анализ и интерпретация результатов. Для более глубокого понимания влияния пробиотика был проведен интегрированный анализ, объединяющий показатели роста, химический состав и динамику продуктивности. Интегрированный анализ (табл. 5) подтверждает, что все наблюдаемые различия являются статистически высокодостоверными (P < 0,001), что исключает вероятность случайных результатов. Высокие значения t-критерия (например, t = 17,00 для прироста массы форели) свидетельствуют о большой величине эффекта и надежности полученных данных.
Таблица 5
Table 5
Комплексный анализ роста, химического состава и динамики продуктивности рыб
Integrated analysis of growth, chemical composition, and dynamics of fish productivity
|
Вид рыбы |
Показатель |
Контрольная группа, г |
Опытная |
Абсолютное |
Относительное различие, % |
Статистические значения* |
Динамика |
Химический |
|
Карп |
Конечная масса |
250 ± 4,8 |
280 ± 5,4 |
30 |
12,0 |
t = 12,78 P < 0,001 |
День 45: 170 → 188 |
Белок: 20.0 → 22,0 (+10 %) Жир: 6,0 → 7,0 (+16,7 %) |
|
Прирост массы |
150 ± 2,8 |
180 ± 3,6 |
30 |
20,0 |
t = 15,32 P < 0,001 |
День 90: 250 → 280 |
||
|
Тиляпия |
Конечная масса |
220 ± 4,5 |
250 ± 5,0 |
30 |
13,6 |
t = 11,45 P < 0,001 |
День 45: 165 → 180 |
Белок: 19,5 → 21,5 (+10,3 %) Жир: 5,8 → 6,8 (+17,2 %) |
|
Прирост массы |
120 ± 2,5 |
150 ± 3,0 |
30 |
25,0 |
t = 13,20 P < 0,001 |
День 90: 220 → 250 |
||
|
Форель |
Конечная масса |
300 ± 6,0 |
330 ± 6,5 |
30 |
10,0 |
t = 14,20 P < 0,001 |
День 45: 200 → 215 |
Белок: 21,0 → 23,0 (+9,5 %) Жир: 6,5 → 7,5 (+15,4 %) |
|
Прирост массы |
200 ± 3,5 |
230 ± 4,0 |
30 |
15,0 |
t = 17,00 P < 0,001 |
День 90: 300 → 330 |
*P – уровень значимости; t – критерий Стьюдента.
Временная динамика, визуализированная на рис. 5, показывает, что статистически значимые различия в массе между группами начали проявляться уже на 45-й день эксперимента и продолжали увеличиваться к 90-му дню, что указывает на кумулятивный и устойчивый эффект пробиотика.
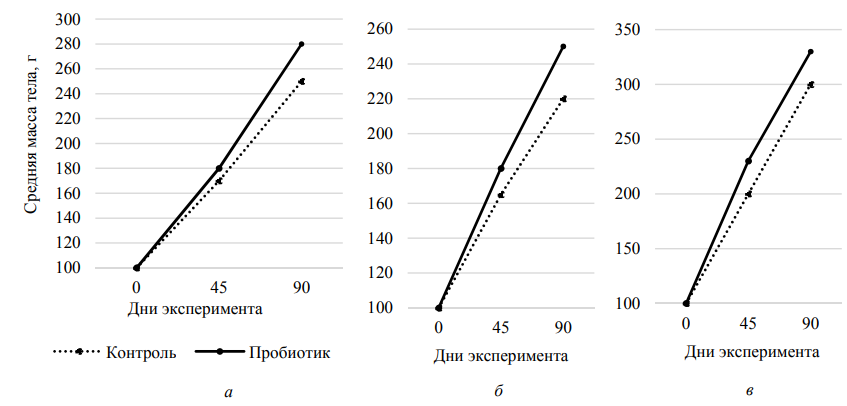
Рис. 5. Временная динамика роста средней массы тела рыб в контрольных и пробиотических группах:
а – карп; б – тиляпия; в – форель
Fig. 5. Temporal dynamics of the growth of the average body weight of fish in the control and probiotic groups:
a – carp; б – tilapia; в – trout
На рис. 5 представлены линейные графики, иллюстрирующие изменение средней массы тела, г, для каждого вида рыб в трех временных точках: в начале (день 0), в середине (день 45) и в конце (день 90) эксперимента. Траектории роста опытных групп (см. рис. 5) начинают расходиться с контрольными и превосходить их уже к середине эксперимента, причем это расхождение увеличивается к его окончанию. Микробиологический анализ кормов и содержимого кишечника. Для подтверждения механизма действия пробиотика был проведен микробиологический анализ кормов и кишечного содержимого рыб. Результаты (табл. 6) демонстрируют успешную колонизацию кишечника полезными бактериями и подавление условно-патогенной микрофлоры.
Таблица 6
Table 6
Комплексный микробиологический анализ кормов и кишечника у карпа
Comprehensive microbiological analysis of feed and intestines in common carp
|
Показатель |
Начало |
Конец |
Конец |
Абсолютная |
Относительная разница, % |
Значение t |
Значение P |
|
Количество бактерий в корме |
|||||||
|
Контроль |
1,23 · 104 |
1,05 · 104 |
– |
–0,18 · 104 |
–14,6 |
5,42 |
<0,01 |
|
Опыт |
8,65 · 107 |
– |
6,93 · 107 |
–1,72 · 107 |
–19,9 |
7,83 |
<0,001 |
|
Количество бактерий в кишечнике карпа |
|||||||
|
Молочнокислые бактерии |
2,35 · 104 |
2,35 · 104 |
6,42 · 106 |
+6,39 · 106 |
+27 191 |
25,83 |
<0,001 |
|
Условно-патогенные бактерии |
7,85 · 104 |
7,85 · 104 |
1,14 · 10³ |
–7,74 · 104 |
–98,5 |
–19,65 |
<0,001 |
Анализ данных табл. 6 выявляет два ключевых аспекта. Во-первых, корм с пробиотиками сохранял высокую концентрацию жизнеспособных бактерий L. acidophilus на протяжении всего эксперимента. Во-вторых, введение пробиотика привело к взрывному росту популяции молочнокислых бактерий и одновременному, почти полному подавлению (на >98 %) условно-патогенных бактерий. Это классический пример конкурентного исключения, когда полезная микрофлора вытесняет вредную, создавая здоровую среду в кишечнике. Таким образом, в опытной группе популяция полезных бактерий на несколько порядков превышает популяцию вредных, в то время как в контрольной группе наблюдается обратная картина.
Сравнительный анализ видоспецифической реакции. Для более глубокого понимания того, как исследуемые виды рыб реагируют на пробиотическую добавку, был проведен сравнительный анализ степени улучшения ключевых показателей. В табл. 7 представлены данные, которые помогают определить наиболее восприимчивые виды и объяснить биологические факторы, влияющие на эту вариабельность.
Таблица 7
Table 7
Различия в реакции разных видов рыб на пробиотики
Differences in fish species’ response to probiotics
|
Вид рыбы |
Показатель |
Контрольная группа |
Опытная |
Абсолютное |
Относительное различие, % |
Значение t |
Значение Р |
|
Карп |
Начальная масса, г |
100 ± 2,0 |
– |
– |
– |
<0,001 |
|
|
Конечная масса, г |
250 ± 4,8 |
290 ± 5,6 |
35 |
13,7 |
13,25 |
||
|
Удельная скорость роста, %/день |
1,55 ± 0,08 |
1,88 ± 0,09 |
0,33 |
21,3 |
7,43 |
||
|
Коэффициент конверсии корма |
1,75 ± 0,10 |
1,45 ± 0,07 |
–0,30 |
–17,1 |
–6,87 |
||
|
Тиляпия |
Выживаемость, % |
87 ± 2,3 |
92 ± 1,8 |
5 |
5,7 |
4,35 |
<0,01 |
|
Начальная масса, г |
100 ± 2,0 |
– |
– |
– |
<0,001 |
||
|
Конечная масса, г |
220 ± 4,5 |
250 ± 5,0 |
30 |
11,3 |
11,58 |
||
|
Удельная скорость роста, %/день |
1,48 ± 0,07 |
1,76 ± 0,08 |
0,28 |
18,9 |
6,53 |
||
|
Коэффициент конверсии корма |
1,82 ± 0,11 |
1,53 ± 0,08 |
–0,29 |
–15,9 |
–5,97 |
||
|
Выживаемость, % |
85 ± 2,1 |
89 ± 1,7 |
4 |
4,7 |
3,82 |
<0,01 |
|
Окончание табл. 7
Ending of Table 7
|
Вид рыбы |
Показатель |
Контрольная группа |
Опытная |
Абсолютное |
Относительное различие, % |
Значение t |
Значение Р |
|
Форель |
Начальная масса, г |
100 ± 2,0 |
– |
– |
– |
<0,001 |
|
|
Конечная масса, г |
300 ± 6,0 |
330 ± 6,5 |
30 |
10,9 |
11,32 |
||
|
Удельная скорость роста, %/день |
1,47 ± 0,07 |
1,76 ± 0,08 |
0,29 |
19,7 |
6,73 |
||
|
Коэффициент конверсии корма |
1,83 ± 0,11 |
1,30 ± 0,07 |
–0,31 |
–18,8 |
–7,10 |
||
|
Выживаемость, % |
83 ± 2,0 |
89 ± 1,7 |
6 |
7,2 |
6,08 |
||
Детальный анализ табл. 7 выявляет тенденцию к улучшению всех показателей у всех видов при использовании пробиотика. У карпа наблюдается наилучшая реакция с точки зрения ускорения роста, зафиксированы наибольшее относительное увеличение удельной скорости роста (+21,3 %) и наилучшее улучшение коэффициента конверсии корма (–17,1 %). С другой стороны, форель продемонстрировала наивысшую реакцию в части улучшения состояния здоровья, показав наибольшее увеличение выживаемости (+7,2 %). Тиляпия показала сбалансированный ответ по всем показателям. Эти различия могут быть связаны с особенностями пищеварительной системы и физиологии каждого вида (рис. 6).
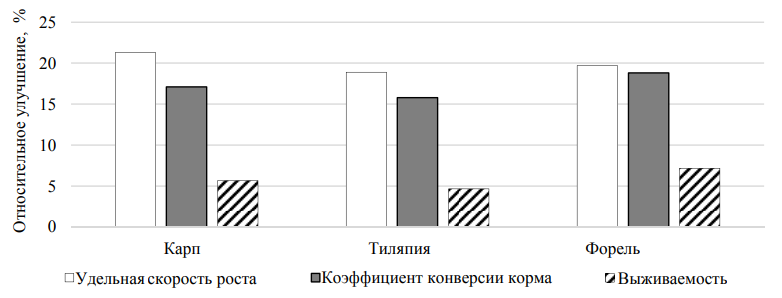
Рис. 6. Сравнение относительного улучшения ключевых показателей продуктивности между тремя видами
Fig. 6. Comparison of relative improvement in key performance indicators among the three species
На графике (см. рис. 6) четко прослеживается, что карп превзошел всех в ускорении роста, а у форели отмечено увеличение выживаемости, что подтверждает наличие видоспецифической реакции.
Корреляционный анализ между показателями роста и химическим составом. Для определения связи ускорения роста с улучшением пищевой ценности рыбы был проведен корреляционный анализ Пирсона, результаты которого приведены в табл. 8.
Таблица 8
Table 8
Коэффициенты корреляции r между показателями роста и химическим составом рыб
Correlation coefficients r between growth indicators and proximate chemical composition of fish
|
Показатель |
Обыкновенный карп |
Нильская тиляпия |
Радужная форель |
|
Корреляция с содержанием белка, % |
|||
|
Прирост массы |
0,89 |
0,86 |
0,88 |
|
FCR |
–0,80 |
–0,77 |
–0,82 |
|
Корреляция с содержанием жира, % |
|||
|
Прирост массы |
0,78 |
0,75 |
0,79 |
|
FCR |
–0,71 |
–0,68 |
–0,74 |
Результаты корреляционного анализа в табл. 8 демонстрируют сильные и статистически высокодостоверные связи. Наблюдается очень сильная положительная корреляция (r приближается к 0,90) между приростом массы и содержанием белка в теле, что математически подтверждает, что ускоренный рост, вызванный пробиотиком, напрямую транслируется в наращивание мышечной ткани, богатой белком. В то же время сильная отрицательная корреляция (r приближается к –0,80) между FCR и содержанием белка означает, что рыба, которая более эффективно использует корм (ниже FCR), имеет и самое высокое содержание белка. Эта связь подтверждает высокую корреляцию экономической эффективности (снижения затрат на корм) с пищевой ценностью конечного продукта.
Заключение
По результатам проведенного исследования установлено, что включение пробиотика L. acidophilus в состав кормов для обыкновенного карпа, нильской тиляпии и радужной форели оказывает комплексное положительное воздействие на их рост, эффективность утилизации корма и физиологическое состояние. Это улучшение связано с успешной колонизацией кишечника полезными микроорганизмами, что привело к подавлению условно-патогенных бактерий и, как следствие, к более эффективному перевариванию и усвоению питательных веществ. Было достигнуто не только ускорение темпов роста, но и значительное снижение кормового коэффициента, что имеет прямое экономическое значение, позволяя снизить себестоимость продукции. Кроме того, повышение содержания белка и жира в теле рыб повышает пищевую ценность конечного продукта для потребителя. В контексте аквакультуры Ирака, сталкивающейся с вызовами в виде высокой стоимости кормов и необходимости повышения устойчивости производства, применение данного пробиотика представляет собой практически значимую и экологически безопасную стратегию. Результаты этой работы служат научным обоснованием для рекомендации широкого внедрения L. acidophilus в промышленные кормовые рецептуры на рыбоводных хозяйствах с целью интенсификации производства и повышения его рентабельности и устойчивости.
1. Abdel-Latif H. M., Abdel-Tawwab M., Khafaga A. F., Dawood M. A. Dietary origanum essential oil improved antioxidative status, immune-related genes, and resistance of common carp (Cyprinus carpio L.) // Aeromonas hydrophila infection, fish & Shellfish Immunology. 2020. V. 104. P. 1–7.
2. Ahmadifar E., Moghadam M. S., Dawood M. A., Hoseinifar S. H. Lactobacillus fermentum and/or ferulic acid improved the immune responses, antioxidative defence and resistance against Aeromonas hydrophila in common carp (Cyprinus carpio) fingerlings // Fish & Shellfish Immunology. 2014. V. 94. P. 916–923.
3. Abdel-Tawwab M., Samir F., Abd El-Naby A. S., Monier M. N. Antioxidative and immunostimulatory effect of dietary cinnamon nanoparticles on the performance of Nile tilapia, Oreochromis niloticus (L.) and its susceptibility to hypoxia stress and Aeromonas hydrophila infection, fish & Shellfish // Immunology. 2018. V. 74. P. 19–25.
4. Hoseinifar S. H., Sun Y. Z., Wang A., Zhou Z. Probiotics as means of diseases control in aquaculture, a review of current knowledge and future perspectives // Frontiers in Microbiology. 2018. V. 9. P. 24–29.
5. Acar Ü., Parrino V., Kesbiç O. S., Lo Paro G., Saoca C., Abbate F., Yılmaz S., Fazio F. Effects of different levels of pomegranate seed oil on some blood parameters and disease resistance against Yersinia ruckeri in rainbow trout // Frontiers in Physiology. 2018. V. 9. P. 596.
6. Adel M., Dawood M. A., Shafiei S., Sakhaie F., She-karabi S. P. Dietary Polygonum minus extract ameliorated the growth performance, humoral immune parameters, immune-related gene expression and resistance against Yersinia ruckeri in rainbow trout (Oncorhynchus mykiss) // Aquaculture. 2020. V. 519. P. 734738.
7. Ajdari A., Ghafarifarsani H., Hoseinifar S. H., Ja-vahery S., Narimanizad F., Gatphayak K., Van Doan H. Effects of dietary supplementation of PrimaLac, inulin, and biomin Imbo on growth performance, antioxidant, and innate immune responses of common carp (Cyprinus carpio) // Aquaculture Nutrition. 2022. P. 8297479.
8. Balta F., Balta Z. D. Preparation of O-antigen from Yersinia ruckeri serotype O1 and use in the slide agglutina-tion test // Journal of Anatolian Environmental and Animal Sciences. 2019. V. 4 (3). P. 480–483.
9. Elumalai P., Kurian A., Lakshmi S., Faggio C., Esteban M. A., Ringø E. Herbal immunomodulators in aquaculture // Reviews in Fisheries Science & Aquaculture. 2020. V. 29 (1). P. 33–57.
10. Ahmadifar E., Pourmohammadi Fallah H., Yousefi M., Dawood M. A., Hoseinifar S. H., Adineh H., Yilmaz S., Paolucci M., Doan H. V. The gene regulatory roles of herbal extracts on the growth, immune system, and reproduction of fish // Animals. 2021. V. 11 (8). P. 2167.
11. Hoseini S. M., Hoseinifar S. H., Doan H. V. Effect of dietary eucalyptol on stress markers, enzyme activities and immune indicators in serum and haematological characteristics of common carp (Cyprinus carpio) exposed to toxic concentration of ambient copper // Aquaculture Research. 2018. V. 49 (9). P. 3045–3054.
12. Hoseini S. M., Hoseinifar S. H., Van Doan H. Growth performance and hematological and antioxidant characteristics of rainbow trout, Oncorhynchus mykiss, fed diets supplemented with Roselle, Hibiscus sabdariffa // Aquaculture. 2021. V. 530. P. 735827.
13. Akanmu O. A., Omitoyin B. O., Emmanuel Ko-lawole A., Emikpe B. O. Effects of dietary lactobacillus fermentum and Saccharomyces cerevisiae on the growth performance, hematological parameters, organ-somatic indices, and protection of Heterobranchus bidorsalis juveniles against Aeromonas hydrophila infection // Journal of Applied Aquaculture. 2020. V. 34 (2). P. 358–381.
14. Assan D., Kuebutornye F. K. A., Hlordzi V., Chen H., Mraz J., Mustapha U., Abarike E. D. Effects of probiotics on digestive enzymes of fish (finfish and shellfish); status and prospects. A mini review // Comparative Biochemistry and Physiology. Part B: Biochemistry and Molecular Biology. 2022. V. 257. P. 110653.
15. Bhatnagar A., Saluja S. Synergistic effects of autochthonous probiotic bacterium and Mentha piperita diets in Catla catla (Hamilton, 1822) for enhanced growth and immune response // Fisheries and Aquatic Sciences. 2019. V. 22 (1). P. 1–14.
16. Heshmati J., Sepidarkish M., Morvaridzadeh M., Farsi F., Tripathi N., Razavi M., Rezaeinejad M. The effect of cinnamon supplementation on glycemic control in women with polycystic ovary syndrome: A systematic review and meta-analysis // Journal of Food Biochemistry. 2021. V. 45 (1). P. 13543.
17. Hoseinifar S. H., Yousefi S., Van Doan H., Ashouri G., Gioacchini G., Maradonna F., Carnevali O. Oxidative stress and antioxidant defense in fish: The implications of probiotic, prebiotic, and synbiotics // Reviews in Fisheries Science & Aquaculture. 2020. V. 29 (2). P. 198–217.
18. Ricker W. E. Growth Rates and Models // Fish Physiology. 1979. V. 8. P. 677–743.
19. Zonneveld N., Huisman E., Boon J. H. The princi-ples of fisheries culture. Jakarta: Gramedia Pustaka, 1991. 318 p.