Россия
УДК 574.2 Организм и среда обитания
УДК 574.5 Гидробиология. Водные биоценозы и экосистемы
Черноморская травяная креветка Palaemon adspersus Rathke, 1836 – единственный промысловый вид из 43 видов десятиногих ракообразных Азово-Черноморского бассейна. Это придонный обитатель верхней части шельфа в водах северо-восточной Атлантики и бассейна Средиземного моря, высокотолерантный вид. Этот бентофаг-полифаг, объект питания рыб, играет важную роль в пищевых цепях водоемов. В условиях интенсивного промысла вида в Азово-Черноморском бассейне важен мониторинг состояния его популяций. Пробы (всего 360 экз. особей) были отобраны из промысловых вентерей у Лебяжьих островов в Каркинитском заливе в сентябре 2016 г. и мае 2017 г. По результатам комплексного лабораторного анализа особей P. adspersus получена характеристика полового состава популяции (на 87–100 % доминировали самки); длина тела у самок достигала 58,1 мм, у самцов – 44,1 мм при длине карапакса до 16,7 и 11,4 мм соответственно. Масса тела креветок варьировала от 0,46 до 3,78 г; большая максимальная масса тела самок соответствовала их более крупным размерам по сравнению с самцами; весовой рост особей тесно связан с линейным ростом (степенная зависимость). Май был временем активного нереста в заливе: многократно преобладали яйценосные самки, большинство из которых недавно отнерестились; встречены яйценосные особи, созревающие повторно, среди самок без яиц около 70 % особей имели созревающие яичники. В сентябре наблюдалось начало «межнерестового отдыха» – самки имели неразвитые яичники и эмбрионов не вынашивали. Синхронизация процессов созревания яичников и развития эмбрионов на плеоподах обеспечивает самкам откладку и вынашивание нескольких кладок яиц за нерестовый сезон. Плодовитость самок достигала 2 263 яйца, длина только что отложенных яиц – 0,72 ± 0,04 мм, объем – 0,15 ± 0,02 мм3; за время инкубации размеры яиц увеличились в 1,2 раза. Максимальный возраст креветки в заливе составлял около 3 лет.
Каркинитский залив, травяная креветка Palaemon adspersus, размер тела, масса тела, созревание, нерест, плодовитость, размеры ооцитов, яиц
Введение
Травяная креветка Palaemon adspersus Rathke, 1836, встречается в верхней части шельфа (0–30 м) в Восточной Атлантике, в Ирландском, Северном, Балтийском морях, морях Средиземного бассейна, Азовском и Черном морях. Этот придонный обитатель (в ночное время поднимается в толщу воды) выдерживает колебания солености воды 2–35 ‰ и температуры 2–25 °C [1]. В черноморских водах Крыма вид предпочитает мелководья лиманов, бухт и заливов до глубины 10 м, с песчаными и илисто-песчаными грунтами, покрытыми зарослями водорослей и морских трав [2–4]. Вид играет важную роль в пищевых цепях: с одной стороны, это бентофаг с широким спектром питания (от детрита и растительных остатков до брюхоногих моллюсков, высших раков и рыбы), с другой – частый пищевой объект рыб, например судака, кутума, воблы, черноспинки [5–9]. Креветку в пищевых целях добывают методом траления с 1978 г.; величина ее вылова в Черном море в 2014–2016 гг. достигала 80–124 т [1, 7]. Кроме того, креветка популярна в виде наживки при рыбной ловле и в качестве корма домашних животных [10]. Все это делает важным мониторинговые исследования ее популяционной биологии, в том числе в Каркинитском заливе.
В литературе имеется информация о таксономическом положении, морфологии, распространении, биотопической приуроченности, особенностях жизненного цикла в разных частях ареала, ряде репродуктивных аспектов травяной креветки [2–6, 8, 9, 11, 12], в том числе и в водах Каркинитского залива (половой и размерный состав, питание, ряд черт репродуктивной биологии) [1, 7, 13]. Данное исследование – часть важных мониторинговых работ по изучению полового состава, размерно-весовой структуры, особенностей воспроизводства промысловой травяной креветки Каркинитского залива. Работа выполнена в рамках научного сотрудничества ФГБОУ ВО «Калининградский государственный технический университет» с Институтом биологии южных морей им. А. О. Ковалевского Российской академии наук (ФИЦ ИнБЮМ, г. Севастополь) и как часть темы ИП НИР КГТУ «Систематика, зоогеография и экология ракообразных Мирового океана» (Рег. № 13.13.029.2).
Материалы и методы исследования
Материалом послужили пробы P. adspersus, собранные в два этапа вентерями с размером ячеи от 6,5 до 8 мм у побережья Лебяжьих островов Каркинитского залива на глубине до 1,5 м в сентябре 2016 г. (239 экз.) и мае 2017 г. (121 экз.) сотрудниками ФИЦ ИнБЮМ. Видовая принадлежность креветок определялась по общепринятым диагностическим ключам [5]. На месте лова материал фиксировался в 4 %-м растворе формальдегида. Методика комплексного лабораторного биологического анализа креветок [14] включала:
– измерение общей длины тела (ДТ, соответствует промысловой длине [1] – от заднего края орбиты глаза до конца тельсона) и длины карапакса (ДК, от заднего края орбиты глаза до середины заднего края карапакса) с точностью 0,1 мм;
– определение индивидуальной массы тела с точностью 0,01 г;
– определение пола особей (по наличию (у самцов) или отсутствию (у самок) придатка appendix masculine на плеоподах второй пары и путем уточнения типа гонад (яичники или семенники, при вскрытии особей));
– оценку степени созревания яичников по 6-балльной шкале (стадии I и II описывают неразвитые яичники неполовозрелых и половозрелых (готовых к первому спариванию) самок, стадии III–V – гонады в начале, середине созревания и зрелые яичники соответственно, стадия VI–II – неразвитые гонады посленерестовых особей);
– оценку степени развития эмбрионов в яйцах на плеоподах по 5-балльной шкале по [14] (стадия 1 описывает только что отложенное яйцо, визуальных признаков развития эмбриона не наблюдается; стадия 2 – заметен зародышевый диск в форме полумесяца, желток занимает до 70 % объема яйца; стадия 3 – около 70 % яйца занято эмбрионом полулунной формы, его хвост может достигать головы и даже заворачиваться на нее, зачаток глаза в виде тонкой серповидной полоски, роговица частично пигментирована; стадия 4 – глаза эмбриона развиты достаточно хорошо, роговица пигментирована, у эмбрионов креветок с крупными яйцами различимы головогрудные придатки; стадия 5 – внутри яйца находится сформированная личинка (эмбриональный науплиус – у пенеоидных креветок; зоэа – у каридных видов, различимо разделение ее тела на головогрудь, сегментированное брюшко и слабо развитые конечности), на этой стадии на плеоподах среди яиц могут встречаться недавно вылупившиеся личинки);
– подсчет абсолютной разовой индивидуальной плодовитости (количества зрелых ооцитов в гонаде у преднерестовых особей, которые будут отложены единоразово во время нереста) и разовой реализованной индивидуальной плодовитости (количества яиц с плеоподов (определялась прямым подсчетом в камере Богорова всех яиц кладки));
– определение размеров зрелых ооцитов и размеров яиц (минимум у 10 особей измеряли длину и ширину зрелых ооцитов и яиц с точностью 0,001 мм, считали средние значения).
При обработке данных использованы методы дескриптивной статистики (описаны экстремумы, среднее значение, стандартное отклонение по выборке), регрессионный анализ выполнен средствами Microsoft Excel методом наименьших квадратов, оценены ряд параметров уравнения размерно-весовой зависимости.
Результаты и обсуждение
Из-за селективности орудий лова (облавливают особей длиной менее 30 мм [1]) в работе представлены данные анализа размерно-полового и весового состава особей травяной креветки в Каркинитском заливе крупнее указанного размера. Это позволяет сравнить их с другими данными, полученными из уловов такими же орудиями. При исследовании половой структуры мы имеем дело с так называемым третичным соотношением полов – соотношением между самцами и самками, устанавливающимся уже среди взрослых животных [15]. В сентябре 2016 г. у исследованных 239 особей P. adspersus соотношение самцов к самкам составило 1 : 7 (13 и 87 % соответственно). Все 121 экз. креветок, собранных в мае 2017 г., были самками. По другим данным [1], только в майских пробах P. adspersus с Каркинитского залива преобладали самцы (69 %); в остальное время (с марта по ноябрь), как и в нашем исследовании, доминировали самки (доля, в среднем, более 90 %). В оз. Донузлав (западное побережье Крыма) в составе уловов также преобладали самки (91–99 %) [13]. Преобладание самок на мелководье залива в теплый период – вероятно, результат раздельного местообитания особей разного пола после оплодотворения: самки мигрируют к берегу, где более высокая температура воды обеспечивает успешный эмбриогенез; самцы в этот период нагуливаются на удалении от берега [1]. В сентябре максимальные и средние размеры (по ДК) самцов были мельче таковых у самок (табл. 1); среди самцов преобладали особи с ДТ до 41 мм, среди самок – особи крупнее 41 мм (рис. 1).
Таблица 1
Table 1
Размеры P. adspersus Каркинитского залива
The size of P. adspersus of the Karkinit Bay
|
Дата |
Самцы |
Самки |
Средний коэффициент |
||||||
|
Общая |
Длина |
Общая |
Длина |
||||||
|
r* |
m ± sd |
r |
m ± sd |
r |
m ± sd |
r |
m ± sd |
||
|
Сентябрь 2016 г. |
33,6–44,1 |
37,3 ± 2,3 |
8,0–11,4 |
9,5 ± 0,7 |
31,5–58,1 |
43,0 ± 5,6 |
8,1–16,7 |
11,8 ± 1,5 |
3,9 |
|
Май |
– |
33,1–56,1 |
43,2 ± 2,4 |
8,3–15,2 |
11,1 ± 0,72 |
3,7 |
|||
* R – диапазон; m – среднее значение; sd – стандартное отклонение по выборке.
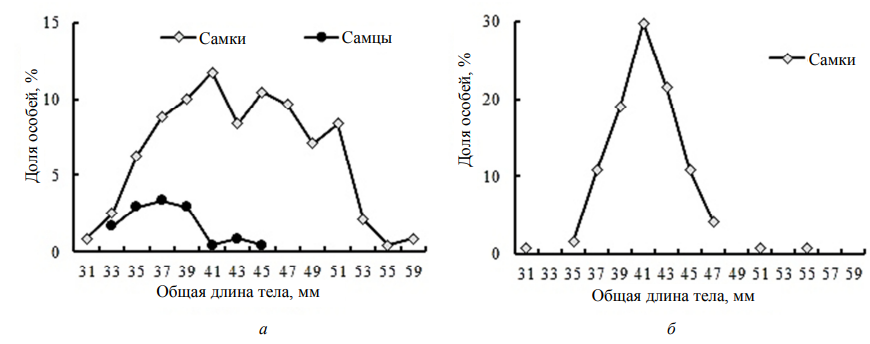
Рис. 1. Размеры тела P. adspersus Каркинитского залива: a – сентябрь 2016 г.; б – май 2017 г.
Fig. 1. Body dimensions of P. adspersus of the Karkinit Bay: a – September 2016; б – May 2017
В мае 2017 г. максимальные размеры самок были чуть меньше, средние размеры сравнимы с таковыми в сентябре 2016 г. (см. табл. 1); унимодальная кривая размерного состава самок показала доминирование особей с модальным размером ДТ 41 мм, по сравнению с сентябрем отмечено уменьшение доли крупноразмерных (ДТ более 45 мм) самок (см. рис. 1).
По другим данным размеры особей P. adspersus в Каркинитском заливе могут достигать больших величин – до 57,3 мм у самцов и до 78,2 мм у самок (табл. 2), по сравнению с нашими данными – до 44,1 и 58,1 мм соответственно.
Таблица 2
Table 2
Размеры тела P. adspersus в разных частях ареала
Body size of P. adspersus in different parts of its range
|
Водоем |
Максимальная общая длина тела, мм |
Источник |
|
Каркинитский залив |
58,1 |
Наши данные |
|
78,2 |
[1] |
|
|
Азово-Черноморский бассейн |
80 |
[1, 5, 6, 9] |
|
Адриатическое море |
72,5 |
[10] |
|
Залив Святого Лаврентия (Канада) |
53,8 |
[4] |
|
Гданьский залив Балтийского моря |
48,5 |
[16] |
Наибольших размеров травяная креветка достигает в Черном и Азовском морях; в Адриатическом море ее максимальные размеры меньше, но крупнее, чем в водах Атлантического океана и Балтийского моря. Масса тела самцов и самок показаны в табл. 3.
Таблица 3
Table 3
Масса тела P. adspersus Каркинитского залива
Body weight of P. adspersus of the Karkinit Bay
|
Дата |
Масса тела, г |
|||
|
самцы |
самки |
|||
|
r |
m ± sd |
r |
m ± sd |
|
|
Сентябрь 2016 г. |
0,55–1,24 |
0,79 ± 0,15 |
0,52–3,78 |
1,43 ± 0,60 |
|
Май 2017 г. |
– |
0,46–2,06 |
1,06 ± 0,36 |
|
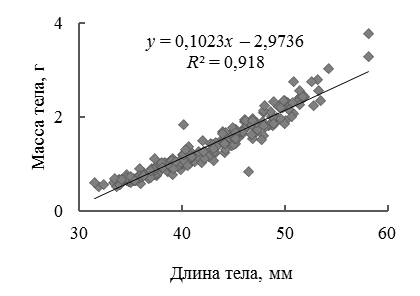
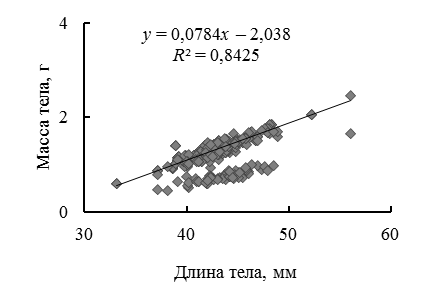
Бóльшая максимальная масса тела самок соответствовала их бóльшим (ДТ до 58,1 мм), по сравнению с самцами (до 44,1 мм), размерам тела. Изучение размерно-весовой зависимости у P. adsperus Каркинитского залива показало сильную линейную связь между параметрами длины и массы тела (рис. 2, табл. 4).
|
|
|
|
||
|
|
а |
б |
||
Рис. 2. Размерно-весовая зависимость у P. adspersus Каркинитского залива:
a – сентябрь 2016 г.; б – май 2017 г.
Fig. 2. Size-weight dependence in P. adspersus of the Karkinit Bay:
a – September 2016; б – May 2017
Таблица 4
Table 4
Результаты регрессионного анализа параметров размерно-весовой зависимости у P. adspersus
Каркинитского залива из проб в 2016 и 2017 г. (уровень значимости 0,05)
Regression analysis of the size-weight dependence parameters in P. adspersus of the Karkinit Bay
from samples in 2016 and 2017 (significance level 0.05)
|
Год |
Параметры анализа |
||||||||||||
|
Коэффициент |
Свободный |
Коэффициент |
F-тест |
Стандартная ошибка b Sb |
Стандартная ошибка a Sa |
t-тест tэмп > tкрит |
Доверительные |
P-значение |
|||||
|
tb |
ta |
tr |
b |
a |
b |
a |
|||||||
|
2016 |
0,1023 |
2,974 |
0,958 |
Fэмп 2652 |
0,0019 |
0,085 |
tэмп 51,50 > tкрит 1,97 |
tэмп 35,08 > tкрит 1,97 |
tэмп 11,27 > tкрит 1,97 |
(0,099; 0,106) |
(2,807; 3,141) |
1,0912 |
8,31 |
|
2017 |
0,0784 |
2,038 |
0,918 |
Fэмп 637 |
0,003 |
0,135 |
tэмп 25,23 > tкрит 1,98 |
tэмп 15,14 > tкрит 1,98 |
tэмп 6,8 |
(0,039; 0,111) |
(1,890; 2,186) |
1,36249 |
1,64384 |
Согласно результатам регрессионного анализа (см. табл. 4) оба уравнения линейной регрессии оказались значимы (оценка с помощью критерия Фишера, F-тест), оценка статистической значимости коэффициентов регрессии и корреляции с помощью t-критерия Стьюдента (t-тест) и доверительных интервалов показателей для обоих лет наблюдений показало: tb > tкрит, ta > tкрит, tr > tкрит, при уровне значимости 0,05 можно признать статистическую значимость параметров регрессии и показателя тесноты связи. Учитывая параметры уравнения зависимости, их доверительные интервалы, можно заключить, что в оба года весовой рост особей достаточно схожим образом несколько превышал линейный рост. По другим данным [1], масса самок P. adspersus в Каркинитском заливе может достигать несколько больших значений (4,65 г), при этом преобладали самки массой 1,38–1,4 г, что сравнимо с нашими сентябрьскими данными.
Репродуктивное состояние самок
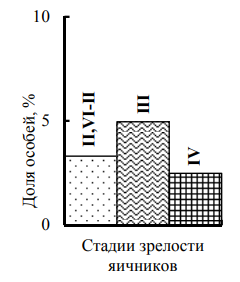
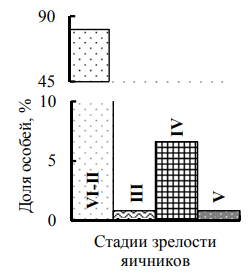
Проба за сентябрь 2016 г. включала самок с гонадами во всех возможных стадиях зрелости, яиц на плеоподах самок не было (рис. 3).
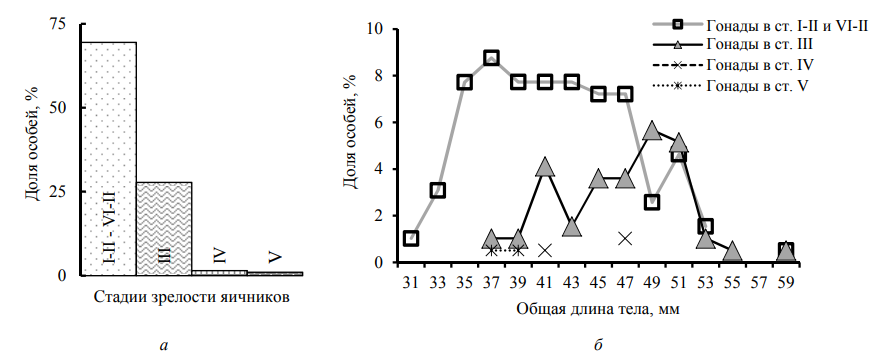
Рис. 3. Репродуктивное состояние самок P. adspersus Каркинитского залива, сентябрь 2016 г.:
a – стадии зрелости яичников; б – размерный состав
Fig. 3. Reproductive status of female P. adspersus of the Karkinit Bay, September 2016:
a – stages of ovarian maturity; б – dimensional composition
Доминировали (почти 70 %) особи с неразвитыми яичниками (стадии зрелости I–II и VI–II); часть из них (36 %) были более мелкими (ДТ 31,5–37 мм) неполовозрелыми (стадия I) или впервые собирающимися созревать самками (стадия II); 34 % самок были более крупными (38–58 мм), находящимися в состоянии «межнерестового отдыха» особями (стадия зрелости VI–II). Оставшиеся 30 % самок составили группу из средне- и крупноразмерных (ДТ 37–58 мм) созревающих (стадии зрелости III и IV) и единичных преднерестовых особей (стадия V); их максимальные размеры были сравнимы с таковыми у особей в межнерестовом состоянии. Можно сделать вывод, что сентябрь 2016 г. в Каркинитском заливе был месяцем завершения нерестового сезона P. adspersus. Для самок с яичниками в начале созревания (стадия зрелости III) и оставшейся меньшей части самок с созревающими гонадами, судя по литературным данным [1], можно предположить миграцию в таком репродуктивном состоянии в ноябре на зимовку в глубоководную часть залива. В майской пробе 2017 г. яйценосные самки многократно преобладали над самками без яиц на плеоподах (89 и 11 % от самок пробы соответственно). Среди самок без яиц с неразвитыми яичниками (3 %) наименьшую ДТ 32–34 мм закономерно имели особи, собирающиеся созревать впервые (стадия зрелости II), а более крупные самки (39–48 мм) были в состоянии «межнерестового отдыха» (стадия зрелости VI–II) (рис. 4).
|
|
|
|
|
а |
б |
в |
|
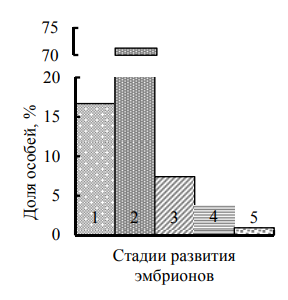
Рис. 4. Репродуктивное состояние самок P. adspersus (Каркинитского залива), май 2017 г.:
Fig. 4. Reproductive status of female P. adspersus of the Karkinit Bay, May 2017: stages of ovarian maturity in females without eggs (a) and oviparous (б); stages of embryo development (в) |
||
|
|
||
|
г |
||
Рис. 4 (окончание). Репродуктивное состояние самок P. adspersus Каркинитского залива, май 2017 г.:
размерный состав (г)
Fig. 4 (ending). Reproductive status of female P. adspersus of the Karkinit Bay, May 2017: size composition (г)
Немного больше (8 %) особей без яиц были среднеразмерными (37–44 мм) созревающими (стадии зрелости III и IV) самками. Преобладали в пробе (81 %) яйценосные особи с неразвитыми гонадами (стадия зрелости VI–II) размерами ДТ 38–56 мм, они составили одну группу с выраженным модальным размером 43 мм. Среди них доминировали недавно отнерестившиеся самки (несли эмбрионы на стадиях развития 1 и 2). У небольшого количества особей эмбриогенез продвинулся до стадий развития 3 и 4 (см. рис. 4). Одна самка (39,8 мм) вынашивала эмбрионы в конечной стадии развития, учитывая ее неразвитые яичники (стадия зрелости VI–II), можно сделать вывод, что она пропускала следующий нерест. Яйценосных особей с созревающими гонадами (стадии зрелости III–V) в мае встречено немного (8 % от самок пробы) (см. рис. 4). Они имели средние размеры (38,9–46,4 мм), вынашивали развивающиеся эмбрионы (в стадиях развития 2–4 с преобладанием стадий 3 и 4). Это были самки, готовящиеся к повторному нересту.
Анализ размерного состава самок P. adspersus в разном репродуктивном состоянии показал: собирающиеся впервые созревать самки (стадия зрелости II) имели ДТ около 33–36 мм, далее, после присущей каридным креветкам линьки полового созревания [17], у них при ДТ 36–40 мм впервые созревали яичники (стадии зрелости III–V). После характерной для каридных креветок преднерестовой линьки [17] самки с ДТ от 38 впервые нерестились и вынашивали яйца.
В целом в мае самки вынашивали на плеоподах эмбрионы на всех возможных стадиях развития (стадии 1–5). Из них 16,7 % (ДТ 38,6–48,5 мм) несли эмбрионы в стадии развития 1; 71,3 % (ДТ 38,1–56,1 мм) – в стадии 2; 7,4 % (ДТ 39,7–44,1 мм) – в стадии 3; 3,7 % (ДТ 38,9–43,1 мм) – в стадии 4; 0,9 % (ДТ 39,8 мм) – в стадии 5 (см. рис. 4). То есть в мае сильно преобладали (88 %) самки, недавно отложившие яйца (стадии 1 и 2). Близкие размеры яйценосных самок – результат того, что самки креветок за время вынашивания эмбрионов не линяют и не растут. Размеры яйценосных самок в Каркинитском заливе, по нашим данным, были меньше, чем таковые, описанные другими авторами (до 63,4 мм) [1].
Можно сделать вывод: в апреле–мае 2017 г. в Каркинитском заливе у P. adspersus наблюдался активный нерест: около 90 % самок несли недавно отложенные яйца, а среди самок без яиц около 70 % особей имели созревающие яичники; в сентябре – конец нерестового сезона. В течение одного сезона по крайней мере часть самок нерестится неоднократно (широкий диапазон размеров самок в «межнерестовом состоянии»; 8 % яйценосных особей имели повторно созревающие яичники), что подтверждают наблюдения для вида разных частей ареала (см. табл. 3). Наши данные о времени нерестового сезона травяной креветки в Каркинитском заливе схожи с другими данными [1]: со второй половины апреля до конца августа – начала сентября, с пиком в мае–июне.
Широкий диапазон размеров яйценосных самок в майских пробах, т. е. в начале нерестового сезона, – следствие растянутого весенне-летнего нереста P. adspersus в заливе каждый год. В других частях ареала сроки репродуктивного периода вида варьируют: в Средиземном море с января по середину июня (пик в апреле); в Балтике – с мая до конца августа (табл. 5).
Таблица 5
Table 5
Нерестовая активность креветок P. adspersus в разных частях ареала
Spawning activity of shrimp P. adspersus in different parts of its range
|
Сроки нереста |
Количество кладок за сезон |
Источник |
|
Каркинитский залив |
||
|
Апрель – сентябрь |
минимум 2 |
Наши данные |
|
Середина апреля – начало сентября |
минимум 2 |
[1] |
|
Балтийское море |
||
|
Май – конец августа |
минимум 2 |
[18] |
|
Средиземное море |
||
|
Январь – середина июня |
минимум 2 |
[6] |
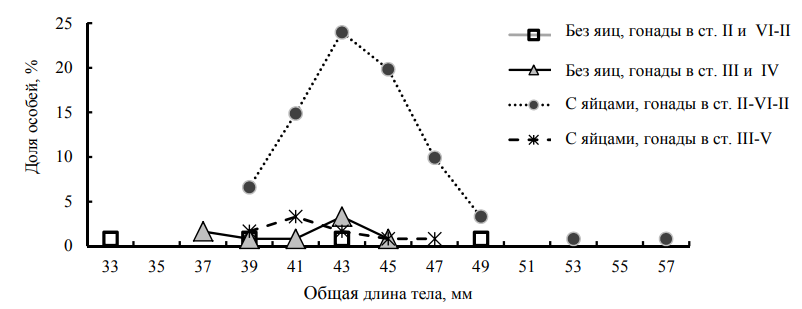
Рис. 5 демонстрирует достаточно синхронное созревание яичников у самок P. adspersus и развитие эмбрионов в яйцах на плеоподах: у 87 % недавно отнерестившихся особей (с эмбрионами в стадиях развития 1 и 2; у единичных особей – в начале стадии 3) гонады были не развиты (стадия зрелости VI–II); меньшая доля самок (8,3 %) имели созревающие и преднерестовые гонады (стадии зрелости III–V) и вынашивали в основном эмбрионы, продвинутые в развитии (стадии 3 и 4).
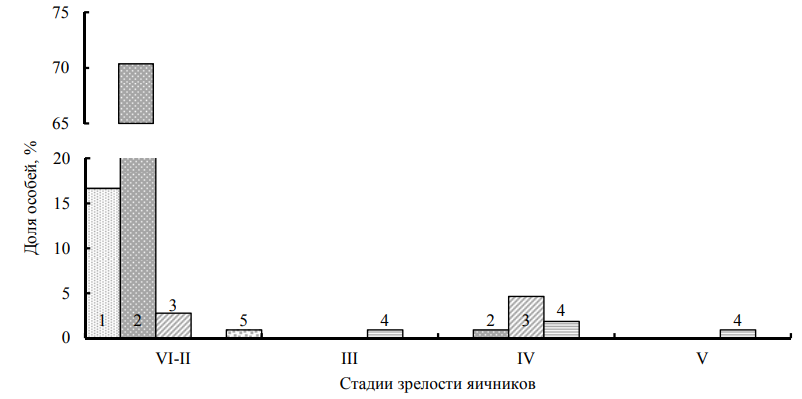
Рис. 5. Стадии развития эмбрионов (стадии 1–5) у самок P. adspersus с яичниками в разных стадиях зрелости
(стадии от VI–II до V) (Каркинитский залив, май 2017 г.)
Fig. 5. Stages of embryo development (stages 1-5) in female P. adspersus with ovaries in different stages of maturity
(stages VI–II to V) (the Karkinit Bay, May 2017)
Единичные самки (5,6 %) пропускали следующий нерест: вынашивая развитые эмбрионы (стадия 5), имели неразвитые яичники (стадия зрелости VI–II). Подобная синхронность созревания гонад и эмбриогенеза, описанная для многих каридных креветок [19], обеспечивает их самкам возможность производить более одной кладки за нерестовый период, используя максимум времени, благоприятного для размножения. По нашим материалам определить длительность инкубации яиц у P. adspersus невозможно. Известно, что у вида в Средиземном и Черном морях она зависит от температуры воды и варьирует от 42 дней до 2 месяцев [6, 18, 20].
Плодовитость, размеры зрелых ооцитов и размеры яиц
Абсолютная разовая плодовитость, определенная у единственной самки P. adspersus с ДТ 43,1 мм, составила 812 зрелых ооцитов со средними размерами 0,575 × 0,625 мм (ширина × длина). Размеры яиц, полученные для 108 самок P. adspersus (ДТ 38,1–56,1 мм) с эмбрионами на разных стадиях развития, показаны в табл. 6.
Таблица 6
Table 6
Плодовитость и размеры яиц P. adspersus Каркинитского залива, май 2017 г.
Fecundity and size of P. adspersus eggs in the Karkinit Bay, May 2017
|
Параметр |
Стадия развития эмбриона |
|||||
|
1 |
2 |
3 |
4 |
5 |
||
|
ДТ, мм |
r |
38,6–48,5 |
38,1–56,1 |
39,7–44,1 |
38,9–43,1 |
39,8 |
|
m ± sd |
43,6 ± 2,4 |
43,8 ± 2,3 |
42,2 ± 1,6 |
40,4 ± 1,5 |
39,8 |
|
|
Плодовитость, |
r |
463–1 742 |
358–2 263 |
491–909 |
489–831 |
579 |
|
m ± sd |
949 ± 336 |
950 ± 329 |
712 ± 178 |
644 ± 147 |
579 |
|
|
Ширина яиц, мм |
r |
0,52–0,68 |
0,62–0,70 |
0,62–0,80 |
0,67–0,80 |
0,68 |
|
m ± sd |
0,64 ± 0,04 |
0,67 ± 0,02 |
0,71 ± 0,05 |
0,76 ± 0,06 |
– |
|
|
Длина яиц, мм |
r |
0,65–0,75 |
0,75–0,90 |
0,8–0,92 |
0,85–0,90 |
0,95 |
|
m ± sd |
0,72 ± 0,04 |
0,78 ± 0,03 |
0,86 ± 0,05 |
0,89 ± 0,03 |
– |
|
|
Объем яиц, мм3 |
r |
0,09–0,18 |
0,15–0,22 |
0,17–0,31 |
0,21–0,30 |
0,23 |
|
m ± sd |
0,15 ± 0,02 |
0,18 ± 0,01 |
0,23 ± 0,05 |
0,27 ± 0,04 |
– |
|
В начале эмбриогенеза размеры яиц составили (0,64 ± 0,04) × (0,72 ± 0,04) мм, почти в конце инкубации (стадия развития эмбрионов 4) они достигли (0,76 ± 0,06) × (0,89 ± 0,03) мм (см. табл. 6). За период инкубации яиц обнаружено увеличение их размеров (как по ширине, так и по длине), при этом в длину яйца увеличились несколько сильнее, чем в ширину (в 1,24 и в 1,19 раза соответственно). Анализ изменения объема яиц за время эмбриогенеза (с 1 по 4 стадию) у P. adspersus Каркинитского залива, по нашим данным, тоже показал его увеличение, в среднем в 1,8 раза (см. табл. 6). По другим данным [20], размеры чуть более мелких яиц у P. adspersus из Синопского залива за время эмбриогенеза увеличились немного меньше – в 1,15 раза по длине и в 1,06 раза по ширине (от 0,739 ± 0,011 до 0,851 ± 0,008 мм по длине и от 0,585 ± 0,005 до 0,622 ± 0,005 мм по ширине). Разовая реализованная плодовитость (РРП) P. adspersus в Каркинитском заливе, по нашим данным, составила 358–2 263 яиц, по другим данным, для вида залива величина плодовитости была схожей [1] (см. табл. 6, 7).
Таблица 7
Table 7
Плодовитость P. adspersus в разных частях ареала
P. adspersus fecundity in different parts of its range
|
Водоем |
Длина тела самок, мм |
Плодовитость, количество яиц, экз. |
|
|
Каркинитский залив (наши данные) |
38,1–56,1 |
358–2 263 |
|
|
Каркинитский залив [1] |
48,0–63,4 |
549–2 281 |
|
|
Синопский залив Черного моря [16] |
51,0–72,0 |
758–3 710 |
В Синопском заливе (южная часть Черного моря) РРП P. adspersus достигала 3 710 яиц, что в 1,6 раза больше ее значений для Каркинитского залива (северная часть моря), но у более крупных самок [16]. Начальная РРП (количество только что отложенных яиц, стадия развития эмбрионов 1) P. adspersus в Каркинитском заливе, по нашим данным, составила 463–1 742 (949 ± 336) яиц у самок размерами 39,1–48,5 мм (см. табл. 6). По другим данным [1], она составила 1 391 ± 513 яйца, но и у более крупных самок (ДТ 48,0–63,4 мм). Отмечена тенденция к росту величины начальной плодовитости с увеличением размеров тела яйценосных особей (рис. 6), прямая пропорциональная зависимость этих показателей описана другими авторами для вида Каркинитского залива [1] и Синопского залива [20].
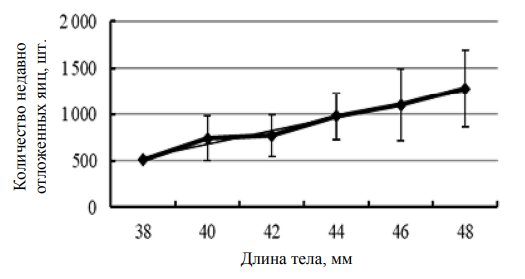
Рис. 6. Начальная разовая реализованная плодовитость P. adspersus Каркинитского залива, май 2017 г.
(обозначены границы доверительных интервалов значений при уровне значимости 0,05)
Fig. 6. Initial one-time realized fecundity of P. adspersus of the Karkinit Bay, May 2017
(the boundaries of the confidence intervals of values with a significance level of 0.05 are indicated)
Разницы в величине плодовитости на разных стадиях эмбриогенеза у P. adspersus Каркинитского залива не выявлено (см. табл. 6), хотя заметна тенденция к уменьшению плодовитости с начала по конец эмбриогенеза. Другие исследователи для вида залива наблюдали определенные потери яиц в процессе вынашивания в зависимости от физиологического состояния самок и условий среды, включая негативное антропогенное воздействие [1]. Зная время инкубации яиц (до двух месяцев), размерный состав и репродуктивное состояние самок, можно предположить, что самки P. adspersus в течение нерестового сезона в Каркинитском заливе могут нереститься 2–3 раза, а учитывая время личиночного и ювенильного периодов жизни, полученные данные опосредованно могут указывать на продолжительность жизни самок травяной креветки в Каркинитском заливе около трех лет. Максимальный возраст для самцов и самок P. adspersus в Адриатическом море также определен как 3 года [10].
Заключение
В теплый период 2016–2017 гг. на мелководье Каркинитского залива в поселениях травяной креветки P. adspersus самки многократно доминировали или самцы совсем не были встречены. У мигрирующих видов креветок это результат раздельного проживания особей разного пола в нерестовый сезон. Размеры креветок в сентябре 2016 г. и мае 2017 г. составили ДТ 31–58 мм при ДК 8–16,7 мм; самцы достигали меньших, чем самки, размеров. В других частях ареала ДТ особей вида может достигать 80 мм. Масса тела особей составила 0,46–3,78 г (1,43 ± ± 0,51 г) при максимальной в других частях ареала до 4,72 г.; средняя масса самцов и самок не отличалась. У травяной креветки растянутый весенне-летний нерестовый сезон. В 2016–2017 гг. у особей в Каркинитском заливе он продолжался с апреля по сентябрь, что дополняет данные других авторов. Возможность откладывать 2–3 кладки в течение нерестового сезона обеспечивается синхронностью процессов созревания яичников и развития эмбрионов, вынашиваемых самками. Плодовитость достигала 2 263 яиц (ДТ самок до 56,1 мм), размер только что отложенных яиц – (0,52–0,68 (0,64 ± 0,04)) × (0,65–0,75 (0,72 ± 0,04)) мм, объем 0,09–0,18 (0,15 ± 0,02) мм3. Отмечена тенденция к увеличению величины плодовитости с увеличением размеров тела самок. За период инкубации яиц (стадии эмбриогенеза 1–4) обнаружено увеличение их размеров примерно в 1,2 раза и наблюдалась тенденция к уменьшению величины плодовитости. Можно предположить продолжительность жизни у P. adspersus в Каркинитском заливе – 3 года.
1. Болтачев А. Р., Статкевич С. В., Карпова Е. П., Хуторенко И. В. Черноморская травяная креветка Palaemon adspersus (Decapoda, Palaemonidae): биология, промысел, проблемы // Вопр. рыболовства. 2017. Т. 18. № 3. С. 313–327.
2. Марин И. Н. Малый атлас десятиногих ракообразных России. М.: Т-во науч. изд. КМК, 2013. 145 с.
3. Аносов С. Е. Характеристика фауны Decapoda Азово-Черноморского бассейна. Качественные и количественные изменения за последнее столетие: автореф. дис. … канд. биол. наук. М.: Изд-во ВНИРО, 2016. 23 с.
4. González-Ortegón E., Sargent P., Pohle G., Martinez-Lage А. The Baltic prawn Palaemon adspersus Rathke, 1837 (Decapoda, Caridea, Palaemonidae): first record, possible establishment, and illustrated key of the subfamily Palaemoninae in northwest Atlantic waters // Aquatic Invasions. 2015. V. 10. Iss. 3. P. 299–312.
5. Кобякова З. И., Долгополова М. А. Отряд десятиногие – Decapoda // Определитель фауны Черного и Азовского морей / отв. ред. В. А. Водяницкий. Киев: Наукова думка, 1969. Т. 2. С. 270–306.
6. Супрунович А. В., Макаров Ю. Н. Культивируемые беспозвоночные. Пищевые беспозвоночные: устрицы, гребешки, раки и креветки. Киев: Наукова думка, 1990. 261 с.
7. Буруковский Р. Н. Состав пищи креветки Palaemon adspersus Rathke, 1837 (Crustacea, Decapoda, Palaemonidae) в Каркинитском заливе Черного моря в сентябре 2016 г. // Мор. биол. журн. 2019. Т. 4. № 1. С. 12–23.
8. Макаров Ю. Н. Десятиногие ракообразные // Фауна Украины. Киев: Наукова думка, 2004. Т. 26. Вып. 1–2. С. 5–427.
9. Holthuis L. B. FAO Species catalogue. Shrimps and prawn of the world // FAO Fish. Synopsis. 1980. V. 1. N. 125. 271 p.
10. Glamuzina L., Conides A., Prusina I., Cukteras M., Klaoudatos D., Zacharaki P., Glamuzina B. Population structure, growth, mortality and fecundity of Palaemon adspersus (Rathke1837; Decapoda: Palaemonidae) in the Parila Lagoon (Croatia, SE Adriatic Sea) with notes on the population management // Turkish Journal of Fisheries and Aquatic Sciences. 2014. N. 14. P. 677–687.
11. Замятина Е. А. Индивидуальная плодовитость травяной креветки (Palaemon adspersus Rathke, 1837) в разных районах Черноморского бассейна // Сб. науч. тр. ЮгНИРО. 2012. Т. 50. С. 123–128.
12. Лисицкая Л. А. Морфометрическая характеристика креветок Palaemon adspersus и Palaemon elegans (Palaemonidae) из черноморских вод юго-западного Крыма (м. Кая-Баш и Балаклавская бухта) // Уч. зап. ТНУ. Сер.: биология, химия. 2012. Т. 25 (64). № 3. С. 109–114.
13. Статкевич С. В. Популяционные характеристики травяной креветки Palaemon adspersus (Rathke, 1837) в Черноморской прибрежной зоне // Промысловые беспозвоночные: VIII Всерос. науч. конф. по промысловым беспозвоночным: материалы докл. Калининград: Изд-во КГТУ, 2015. C. 129–130.
14. Sudnik S. A., Falkenhaug T. The method of biological analysis for caridean shrimps (Decapoda: Natantia: Caridea) with emphasis on pelagic shrimps // Наука и общество в условиях глобализации: материалы Междунар. науч.-практ. конф. (Уфа, 21–22 апреля 2014 г.). Уфа: РИО ИЦИПТ, 2014. С. 7–11.
15. Кауфман З. С. Эволюция размножения пола: в 2 т. Петрозаводск: Изд-во КарНЦ РАН, 1994. Т. 2. 190 с.
16. Lapińska E., Shaniawska A. Environmental prefer-ences of Crangon crangon (Linnaeus, 1758), Palaemon adspersus Rathke, 1837, and Palaemon elegans Rathke, 1837, in the littoral zone of the Gulf of Gdańsk // Crusta-ceana. 2006. V. 79. N. 6. P. 649–662.
17. Судник С. А. О связи линочного и репродуктивного циклов у самок креветок (Crustacea, Decapoda, Natantia) // Водные биоресурсы, аквакультура и экология водоемов: тр. науч. конф. Калининград: Изд-во КГТУ, 2013. С. 290–293.
18. Klaoudatos S., Tsevis N. Biological observations on Palaemon adspersus (Rathke) at Messolonghiilagoon // Thalassographica. 1987. N. 10. P. 73–88.
19. Судник С. А. Эволюционные аспекты репродуктивных стратегий креветок // Уч. зап. Казан. ун-та. Сер.: Естественные науки. 2017. Т. 159. Кн. 3. C. 443–455.
20. Bilgin S., Samsun O. Fecundity and egg size of three shrimp species, Crangon crangon, Palaemon adspersus and Palaemon elegans (Crustacea: Decapoda: Caridea), off Sinop Peninsula (Turkey) in the Black Sea // Turk. J. Zool. 2006. V. 30. P. 413–421.