Россия
Россия
Трансформация дельтовой экосистемы, происходящая на протяжении многих лет, может приводить к изменениям всех составных частей биотопа. Для оценки обстановки в дельте Волги проведены иссле-дования рыб методом неполного паразитологического анализа. За пятилетний период (2019–2023 гг.) состав паразитов, способных вызывать развитие инвазионных заболеваний у промысловых видов рыб дельты Волги, включал представителей класса Cestoda, Nematoda, Acanthocephala, Crustacea. Наибольшая встречаемость заболеваний зарегистрирована в весенний период, что определено биологическими особенностями гельминтов – возбудителей болезней, в то же время эколого-трофический фактор являлся ведущим при формировании эпизоотически значимой фауны паразитов (цестоды, нематоды, скребни), развитие которых сопряжено с наличием промежуточных хозяев и продолжительностью паразитирования. Гидролого-гидрохимические показатели определяли встречаемость специфичного для сазана скребня Pomphorhynchus laevis и патогенного рачка Achtheres percarum. Инвазионные болезни протекали в субклинической форме, проявляясь общепатологическими реакциями в организме пораженных рыб. Выявляемые уровни заболеваемости носили неоднородный характер, однако за период исследования состав таксонов (возбудителей болезней) не претерпел существенных изменений. В большинстве случаев заболеваемость обследованных рыб находилась в пределах фоновых показателей с некоторым увеличением в отдельные годы, исключение составил эустронгилидоз окуня. Систематическое выявление постоянного круга паразитов, провоцирующих развитие патологических изменений в органах и тканях своих хозяев, а также низкий уровень заболеваемости, не превышающий среднемноголетний показатель, свидетельствуют о стабильно протекающих инвазионных процессах и сохранении механизмов передачи возбудителя в гидробиоценозе дельты Волги.
инвазии, болезни рыб, дельта Волги, цестодозы, нематоды, возбудители, патологические изменения
Введение
Водный режим служит показателем благополучия/неблагополучия для воспроизводства рыб и развития заселяющих их паразитических форм. На фоне продолжительной антропопрессии изменились условия обитания рыбного сообщества, что стало причиной перестройки и в структуре популяции паразитов. Динамика степени инвазированности рыб определяется факторами, обуславливающими сезонные изменения фауны паразитов, численность промежуточных, дополнительных и дефинитивных хозяев [1]. Современная устойчивая тенденция часто формирующихся маловодных периодов в Волго-Каспийском бассейне естественным образом регулирует жизненные циклы паразитов и отбор в паразитарной системе. Условия паводка в низовьях р. Волги зависят от попусков воды Волжской ГЭС. Зарегулирование волжского стока привело к нарушению распределения стока р. Волги по сезонам и продолжительности обводнения нерестилищ. Изменились сроки прохождения максимальных расходов воды: если до зарегулирования волжского стока они отмечались в среднем в первой декаде июня, то в современный период осуществляются на месяц раньше. Это негативно отражается на условиях нагула и эффективности воспроизводства основных видов рыб [2]. Изменения дельтовых биотопов, безусловно, отражаются и на видовом составе фауны паразитов рыб. Благополучное существование паразита в данной акватории возможно лишь при сочетании всего комплекса условий, необходимых для него на разных этапах жизненного цикла. Отсутствие хотя бы одного из необходимых факторов при наличии всех прочих может повлечь за собой исчезновение паразита в данном биотопе [3, 4]. Гельминты рыб, имеющие сложный цикл развития, достоверно отображают изменения в биоценозе водоемов: динамику численности и биомассы зоопланктона и зообентоса, зарастание литоральной зоны, трансформации в составе ихтиоценоза [5]. Присутствие различных видов ихтиопаразитов указывает на состав сообществ зоопланктона и макрозообентоса, организмы которых являются промежуточными хозяевами паразитов [6, 7]. Паразитологические данные о численности и разнообразии паразитов, изменении численности промежуточных и окончательных хозяев являются важными биоиндикационными показателями, позволяющими оценить состояние и тенденции изменения природных комплексов [1]. Исследования фауны паразитов являются одним из актуальных, но недостаточно освоенных направлений в решении проблемы инвазий [8–10]. Инвазионные болезни, вызываемые цестодами сем. Triaenophoridae и сем. Proteocephalidae, а также нематодами сем. Dioctophymidae, выявляются во многих водоемах России среди разных представителей ихтиофауны, однако информации об этом недостаточно. В отдельных районах зараженность данными гельминтами может достигать значительного уровня, поэтому проведение контроля за зараженностью рыб обосновано и крайне важно. В настоящее время инвазионные процессы обретают все более регулярный характер в различных зоогеографических зонах. В этой связи целью работы явилось изучение эпизоотической ситуации в дельте Волги на современном этапе.
Материал и методы исследования
В течение пяти лет (2019–2023 гг.) весной, летом и осенью проводили паразитологическое обследование половозрелых леща, сазана, сома, щуки, судака и окуня. За указанный период направленному неполному паразитологическому исследованию подвергнуто 5 854 экз. рыб. Отбор материала осуществляли на рыбопромысловых участках Главного и Белинского банков дельты Волги. С применением стереоскопических и биологических микроскопов исследовали жабры, органы полости тела и мышцы представителей ихтиофауны. Исследование было направлено на выявление паразитических организмов, вызывающих развитие патологических процессов клинического и субклинического уровней [11, 12]. Выявленных и изолированных возбудителей идентифицировали до вида [13, 14] с использованием стереоскопических (МБС-10) микроскопов. Рассчитывали паразитологические показатели зараженности: экстенсивность инвазии, интенсивность инвазии, индекс обилия. Полученные результаты обрабатывали статистически в программе Microsoft Excel 2010. Использовали методы непараметрической статистики. Среднемноголетний показатель рассчитывался за период 2000–2023 гг.
Результаты и обсуждение
По результатам паразитологических исследований в дельте р. Волги у половозрелых промысловых видов рыб зарегистрированы гельминты, инициировавшие развитие инвазионных заболеваний: Proteocephalus osculatus (Cestoda: Proteocephalidae), Caryophyllaeus laticeps, Caryophyllaeus fimbriceps (Cestoda: Caryophyllaeidae), Raphidascaris acus (Nematoda: Anisakidae), Eustrongylides excisus (Nematoda: Dioctophymidae), Pomphorhynchus laevis (Acanthocephala: Pomphorhynchidae), Achteres percarum (Crustacea: Lernaeopodidae). Максимальное разнообразие инвазионных процессов у рыб приходилось на весенний период, что обусловлено биологией развития возбудителей и температурным режимом, формировавшимся на акватории, ускоряющими (либо лимитирующими) процессы созревания и исхода одногодичных гельминтов: P. osculatus, C. laticeps, C. fimbriceps, R. acus. В группу потенциальных возбудителей цестодозов также входил Triaenophorus nodulosus (Cestoda: Triaenophoridae), провоцирующий триенофороз щуки, однако данное заболевание в исследуемый период выявляли нерегулярно, а в последние два года не отмечали, в то время как частота встречаемости сома, леща и сазана, инвазированных, соответственно, P. osculates, C. laticeps и C. fimbriceps, напротив, имела тенденцию к росту. Уровни заболеваемости цестодозами с 2019 по 2023 г. характеризовались разнонаправленностью, но находились в пределах ошибки среднемноголетнего значения (1,66 ± 0,21 и 1,06 ± 0,34 % кариофиллез леща и сазана соответственно, 2,03 ± 0,25 % протеоцефалез сома, 0,92 ± 0,27 % триенофороз щуки), т. е. оставались в границах фоновых величин. Высокие уровни цестодозов отмечали у сазана в 2019 г., у сома в 2020 г., у леща в 2022 г. Интенсивность инвазии цестодами варьировала в широком диапазоне: 12–228 экз. на рыбу. Субклинические признаки заболевания проявлялись воспалительными реакциями и нарушением процессов кровообращения (рис. 1).

|
|
|
|
|
Рис. 1. Нарушения в кишечнике рыб, пораженном цестодами:
Fig. 1. Disorders in the intestines of fish affected by cestodes: small-focal hemorrhages on the intestinal mucosa |
||
В некоторых случаях патогенное воздействие гельминтов проявлялось в сужении просвета кишечника вплоть до полной непроходимости. Подобная картина была характерна для каждого проявления цестодоза у леща, сазана, сома и щуки на протяжении всего периода исследований.
Частота встречаемости щуки, пораженной рафидаскаридозом в 2019–2023 гг. периодически изменялась, но не превышала ошибки среднемноголетнего показателя (1,07 ± 0,19 %), интенсивность составляла 8–38 экз. Наибольший уровень болезни выявлен в 2023 г., вероятно, это обусловлено ранним паводком и увеличением температуры воды в данный период, что благотворно сказалось на развитии нематод (рис. 2).
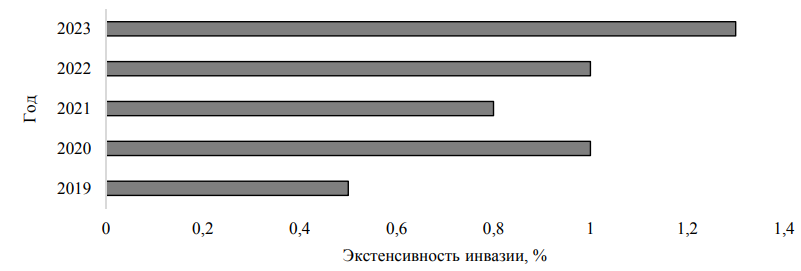
Рис. 2. Динамика заболеваемости щуки рафидаскаридозом (2019–2023 гг.)
Fig. 2. Dynamics of pike disease caused by Rafidaskariosis (2019-2023)
При сравнении экстенсивности инвазии нематодами R. acus и температурного режима в основном русле дельты Волги весной 2019–2023 гг. было установлено, что уровень зараженности рафидаскарисом щуки имел тесную связь с температурой воды (r = 0,943). Возбудитель R. acus относится к теплолюбивым паразитам, и при повышении температуры воды, как правило, в весенний период онтогенез круглых червей активизируется. Нематоде свойственен чрезвычайно широкий круг промежуточных хозяев, относящихся к разным типам и классам гидробионтов: олигохеты, моллюски, ракообразные, личинки насекомых и др. Мирные рыбы выполняют роль дополнительных хозяев; резервуарными хозяевами являются хищные рыбы и личинки некоторых насекомых, способные аккумулировать рафидаскаридозных личинок.
За счет особого строения головной части личинки совершают миграции из кишечника в полость тела своего хозяина, данная способность гельминта указывает на морфобиологические адаптации паразита. Чрезвычайно широкий круг промежуточных и резервуарных хозяев у R. acus служит показателем выгодной адаптации для паразита, обеспечивающей широкое распространение в пресноводных водоемах.
Патологические изменения в пищеварительном тракте щуки при рафидаскаридозе характеризовались проявлением локального отека и разноочаговой гиперемией слизистой оболочки стенок кишечника. Данные нарушения приводят к снижению интенсивности всасывания, но не препятствуют прохождению пищевых масс, в отличие от скопления цестод, т. к. высокая подвижность нематод не способствует образованию пробки в кишечнике.
Патологические процессы, обусловленные инвазией P. osculatus, C. laticeps, C. fimbriceps, R. acus, часто приходятся на последний жизненный этап этих паразитических организмов, что исключает длительное развитие болезни и усугубление патологии. В группе возбудителей нематодозов регулярно регистрировали широко распространенных в регионе диоктофимид – E. excisus, способных вызывать развитие патологических изменений в различных органах и тканях организма хозяина. Нематодозы, провоцируемые круглыми червями рода Eustron-
gylides, зарегистрированы у хищных рыб – сома и окуня. Личинки гельминтов у окуня находились во внутренних органах и в мышечной ткани, вызывая нарушение ее структуры, атрофию, перфорацию пораженных органов. Инвазия паренхиматозных органов сопровождалась абсцессом и гиперемией. У сома эустронгилидесы локализовались в полости тела, на брыжейке и в стенке желудка, приводя к развитию мелкоочаговой гиперемии слизистой оболочки и гнойного воспаления в мышечном слое стенок органа.
Эустронгилидоз отмечали ежесезонно в среднем у 6,04 % окуня и 2,08 % сома, что указывало на некоторое превышение среднемноголетнего значения у окуня (5,14 ± 0,37 %) и снижение у сома (3,19 ± 0,56 %). Интенсивность заражения составляла 16–75 экз. у окуня и 58–96 экз. у сома. Максимальный показатель заболеваемости эустронгилидозом отмечен у окуня в 2021 г. В популяции окуня процент пораженных особей достоверно выше (U = 0,5, p ≤ 0,05), чем у сома. Различие уровня заболеваний у данных хищных рыб обусловлено способами передачи возбудителя по трофической цепи. Наличие трех хозяев в жизненном цикле E. excisus и длительный период его паразитирования в рыбе обеспечивают диапазон ежегодного изменения уровней заражения и болезни представителей ихтиофауны.
В период исследований также регистрировали поражение сазана специфичным скребнем P. laevis. Уровень помфоринхоза был ниже среднего многолетнего значения (1,65 ± 0,47 %), интенсивность инвазии варьировала от 18 до 110 экз. Максимум заболеваемости отмечен в 2021 г. Результаты исследований показали, что в периоды с активной мелиорацией или повышенным стоком воды, когда увеличивается проточность водоема и содержание кислорода, заражение скребнем приобретает более массовый характер. Этим объясняются низкие показатели заболеваемости сазана в последние маловодные годы (2022–2023 гг.).
Признаки помфоринхоза сазана выражались в возникновении воспалительной реакции слизистой оболочки кишечника, множественных уплотненных по периферии прободениях в местах внедрения скребней и мелкоочаговых кровоизлияний.
Постоянным сочленом инвазионного сообщества являлись и ракообразные A. percarum, вызывавшие нарушения функции жаберного аппарата у судака в единичных случаях, что соответствовало среднемноголетнему значению 0,52 ± 0,16 % (2008–2023 гг.). Максимальный уровень ахтериоза у данного вида рыб выявлен в 2019 г. Кроме жабр, патогенного рачка обнаруживали в ротовой полости рыб, однако патологических изменений в тканях верхнего неба, языка и подъязычной области не обнаружено. Подобное мало характерное местообитание паразита, возможно, связано с неблагоприятной экологической обстановкой в водоеме, когда паразит стремится найти более подходящую для нормальной жизнедеятельности эконишу.
Выявленный ахтериоз протекал на субклиническом уровне, сопровождаясь очаговым некрозом тканей жаберных лепестков и воспалительными реакциями. Отсутствие признаков заболевания в отдельные годы связано с развитием возбудителя. Как правило, низкие температура воды и кислород отрицательно влияют на плодовитость рачка, что тормозит онтогенез паразита и отражается на его численности. Кроме того, изменения зараженности рыб ракообразными могут быть вызваны токсикологической обстановкой водоема [15].
Сравнительный анализ многолетних результатов исследований показал, что встречаемость наиболее распространенных эпизоотически значимых паразитов у представителей ихтиофауны Волго-Каспийского бассейна несколько изменилась. За последние 23 года снизилась численность цестод T. nodulosus и P.osculatus и, напротив, выросли количественные показатели инвазии личинками круглых червей E. excisus.
Заключение
В целом за последние 5 лет (2019–2023 гг.)
у половозрелых полупроходных и речных рыб (щуки, сома, судака, окуня, леща и сазана) на промысловых участках дельты Волги выявлены заболевания паразитарной природы, наибольшее проявление которых отмечено в весенний период. Видовой состав возбудителей был представлен следующими паразитическими организмами: P. osculatus, C. laticeps, C. fimbriceps, R. acus, T. nodulosus, E. excisus, P. laevis, A. percarum. Более 20 лет (2000–2023 гг.) видовой состав паразитических организмов, вызывающих развитие субклинической патологии у промысловых рыб, сохранял относительное постоянство. При этом уровень развития заболеваний, инициированных одногодичными паразитами, не превышал границы среднемноголетнего значения. Эустронгилидоз, возбудитель которого отличается триксенным циклом развития и устойчивостью к воздействию параметров среды второго порядка, несколько превысил фоновый показатель. Все выявленные инвазионные заболевания протекали на субклиническом уровне.
Видовое разнообразие возбудителей и межгодовые колебания уровня заболеваемости в период исследования, как и в целом в 2000–2023 гг., определялись следующими факторами: водно-термическим режимом, трофическими условиями биотопов, продолжительностью паразитирования в рыбе, а также поголовьем окончательных хозяев. Невысокие и относительно стабильные показатели развития субклинических патологических инвазионных процессов, не превышающие фоновых значений, свидетельствовали о формировании устойчивых паразитохозяинных отношений в популяции обследованных рыб и указывали на стабильную эпизоотологическую ситуацию в дельте Волги.
1. Иванов В. М., Семенова Н. Н., Калмыков А. П. Гельминты в экосистеме дельты Волги. Трематоды: моногр. Астрахань: Волга, 2012. Т. 1. 255 с.
2. Чавычалова Н. И., Тарадина Д. Г., Васильченко О. М., Муханова Р. С. Состояние естественного воспроизводства полупроходных и речных рыб в низовьях Волги // Материалы Всерос. науч. конф. с междунар. участием, посвящ. 100-летию Астрахан. гос. заповед. Астрахань: Мир, 2019. С. 121–123.
3. Романова Е. М., Индирякова Т. А., Игнаткин Д. С., Баева Т. Г. Экологический мониторинг биобезопасности хозяйственно развитых территорий. Ульяновск: Изд-во УлГАУ им. П. А. Столыпина, 2015. 186 с.
4. Романова Е. М., Игнаткин Д. С., Романов В. В., Шадыева Л. А., Шленкина Т. М. Биологический кон-троль окружающей среды в зонах повышенной антропогенной нагрузки: моногр. Ульяновск: Изд-во УлГАУ им. П. А. Столыпина, 2015. 240 с.
5. Аникиева Л. В., Иешко Е. П., Румянцев Е. А. Эко-логический анализ гельминтов ряпушки и корюшки Онежского озера // Тр. Карельс. науч. центра РАН. Сер.: Экологические исследования. 2016. № 4. С. 37–47. DOIhttps://doi.org/10.17076/eco250.
6. Шабунов А. А., Радченко Н. М. Паразиты рыб, земноводных и чайных птиц в экосистемах крупных водоемов Вологодской области. Вологда: Изд-во ВоГТУ, 2012. 243 с.
7. Рубанова М. В., Мухортова О. В., Поддубная Н. Я. Динамика фауны гельминтов пищеварительного тракта Perca fluviatilis (Actinopterygii: Perciformes) и ее взаимосвязь с зоопланктоном Национального парка «Самарская Лука» // Nature Conservation Research. Заповедная наука. 2020. № 5 (1). С. 64–86. https://dx.doi.org/10.24189/ncr.2020.009.
8. Dunn A. M. Parasites and biological invasions // Advances in Parasitology. 2009. V. 68. P. 161–184. DOIhttps://doi.org/10.1016/S0065-308X(08)00607-6.
9. Jones C. M., Brown M. J. F. Parasites and genetic diversity in an invasive bumblebee // Journal of Animal Ecology. 2014. V. 83 (6). P. 1428–1440. DOIhttps://doi.org/10.1111/1365-2656.12235.
10. Poulin R. Invasion ecology meets parasitology: Advances and challenges // International Journal for Parasitology: Parasites and Wildlife. 2017. V. 6 (3). P. 361–363. DOIhttps://doi.org/10.1016/j.ijppaw.2017.03.006.
11. Мусселиус В. А., Ванятинский В. Ф., Вихман А. А. Лабораторный практикум по болезням рыб. М.: Лег. и пищ. пром-сть, 1983. 296 с.
12. Быховская-Павловская И. Е. Паразиты рыб: рук. по изучению. Л.: Изд-во Акад. наук СССР, 1985. 121 с.
13. Определитель паразитов пресноводных рыб СССР / под ред. И. Е. Быховской-Павловской, А. В. Гусева, М. Н. Дубининой, Н. А. Изюмовой. М.; Л.: Изд-во Акад. наук СССР, 1962. 776 c.
14. Определитель паразитов пресноводных рыб фауны СССР / под ред. О. Н. Бауера. Л.: Наука, 1987. Т. 3. Паразитические многоклеточные. 583 с.
15. Богданова Е. А. Паразиты рыб как биоиндикаторы токсикологической ситуации в водоеме: метод. пособие. СПб.: Изд-во ГосНИОРХ, 1993. 27 с.